Лишний вес от почек
Содержание статьи
Ожирение бьет по почкам
15 февраля 2018
Врач-уролог Центра женской урологии Плеханова Ольга призывает быть настороже и предупредить неотвратимое поражение почек, связанное с избыточной массой тела.
В 2017 г. Всемирный день здоровья почек посвящен проблеме ожирения. Эксперты призывают быть настороже и предупредить неотвратимое поражение почек, связанное с избыточной массой тела.
Всемирный день почки отмечается ежегодно — во 2-й четверг марта. Как отмечается на официальном сайте, актуальность мероприятия обоснована эпидемиологией: патология почек сопоставима с такими социально значимыми
заболеваниями, как гипертоническая болезнь и сахарный диабет. Каждый 10-й житель Земли имеет хроническую болезнь почек (ХБП, ранее использовался термин хроническая почечная недостаточность). Ежегодно миллионы людей умирают преждевременно от инфарктов и инсультов, связанных с ХБП.
Ожирение почек
Эпидемиология заболеваний почек на фоне ожирения стремительно меняется. Так, по данным серии аутопсий, проведенных в США, встречаемость гломерулопатии, индуцированной ожирением, возросла в 10 раз, от 0,2% в 1986–1990 гг. до 2% в 1996–2000 гг.
По данным Hsu C.Y. и группы авторов, у людей с индексом массы тела (ИМТ), превышающим 30 кг/м2, риск развития терминальной хронической почечной недостаточности увеличивается в 3 раза по сравнению с пациентами с нормальной массой тела. Люди с избыточной массой тела могут страдать от недостатка мышечной массы и дефицита белка, последний – ассоциируется с плохим прогнозом у пациентов с ХБП [2].
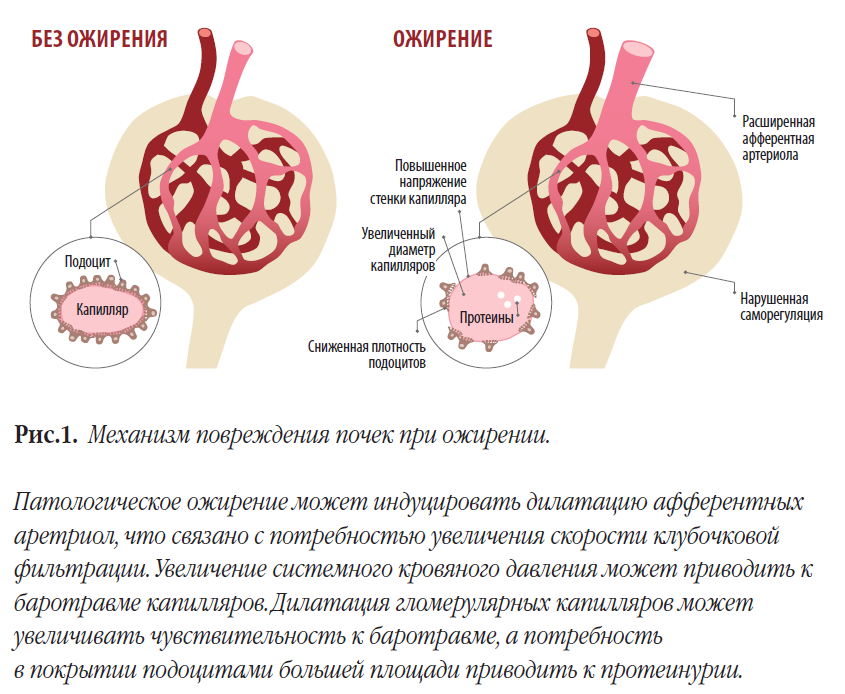
По мнению проф. Kumar Sharma, прогнозы на перспективу неутешительны: частота нефропатий, связанных с ожирением, будет только расти, в первую очередь это связано с потреблением высококалорийной переработанной пищи на фоне снижения физической активности. Значимую роль играет возросшее потребление переработанных и консервированных продуктов с высоким содержанием соли, с чем связано развитие гипертензии и усиление оксидативного стресса.
«Следует отметить, что ассоциация между ожирением и нарушением функций почек сохраняется даже при поправке на метаболические и сердечно- сосудистые осложнения, связанные с избыточной массой тела, — пишет Csaba P. Kovesdy et al. [3]. — Ожирение влияет на здоровье почек посредством в том числе механизмов, частично не связанных с этими осложнениями». Более того, негативное влияние ожирения более масштабно – вплоть до ассоциации с нефролитиазом и злокачественными новообразованиями.
Патофизиологические механизмы
Один из главных механизмов, лежащих в основе патофизиологии ожирения и ХПБ, — это воспаление. Установлено, что почка и жировая ткань секретируют такие провоспалительные медиаторы, как ангиотензин II и лептин, которые в свою очередь могут воздей-ствовать на подоциты, мезангиальные клетки и клетки собирательных трубочек. Подоциты несут на своей поверхности рецепторы к инсулину и лептину, играющие важную роль в поддержании механизма селективной проницаемости. Высокий уровень лептина и адипонектина, характерный для ожирения, может провоцировать провоспалительные реакции со стороны иммунной системы.
По данным Anders и других авторов, один из факторов, поддерживающих процесс воспаления при ХБП на фоне ожирения, — состояние микробиоты кишечника. Согласно современным представлениям, существует прямая связь между ожирением и составом микрофлоры кишечника. Изменения микробиоты могут приводить к нарушению проницаемости кишечной стенки, кишечного гомеостаза и высвобождению клеток иммунной системы, вырабатывающих провоспалительные цитокины.
Более того, уремические токсины, вырабатываемые кишечной микрофлорой, играют роль в патогенезе формирования инсулиновой резистентности. В свою очередь, воспаление, индуцированное ХБП, способствует активизации иммунных клеток жировой ткани и стимулирует адипоциты, что в конечном итоге может приводить к ожирению.
Интересен тот факт, что взаимодействие желудочно-кишечного тракта (ЖКТ) и почек на гуморальном уровне лежит в основе регуляции натриевого обмена. Так, поступающий с пищей натрий активирует натриевые каналы G-клеток желудка, что сопровождается выработкой гастрина и допамина, ингибирующих транспорт натрия в собирательных трубочках, усиливая выведение натрия с мочой. У пациентов с ожирением наблюдается нарушение этого регуляторного механизма, что вызывает артериальную гипертензию и оказывает повреждающее действие на почки.
Жировая ткань как эндокринный орган продуцирует помимо лептина такие биологически активные вещества, как ангиопоэтины, сосудистый эндотелиальный фактор роста, катепсины, адипонектин и резистин. Данные вещества могут вызывать гипертрофию клеток, накопление межклеточного матрикса и фиброз почечной ткани.
По данным Hunley T.E. [4], изучавших в составе группы авторов взаимосвязь между ожирением и почечной недостаточностью, жировые клетки и макрофаги жировой ткани способны вырабатывать ангиотензин и ангиотензиноген.
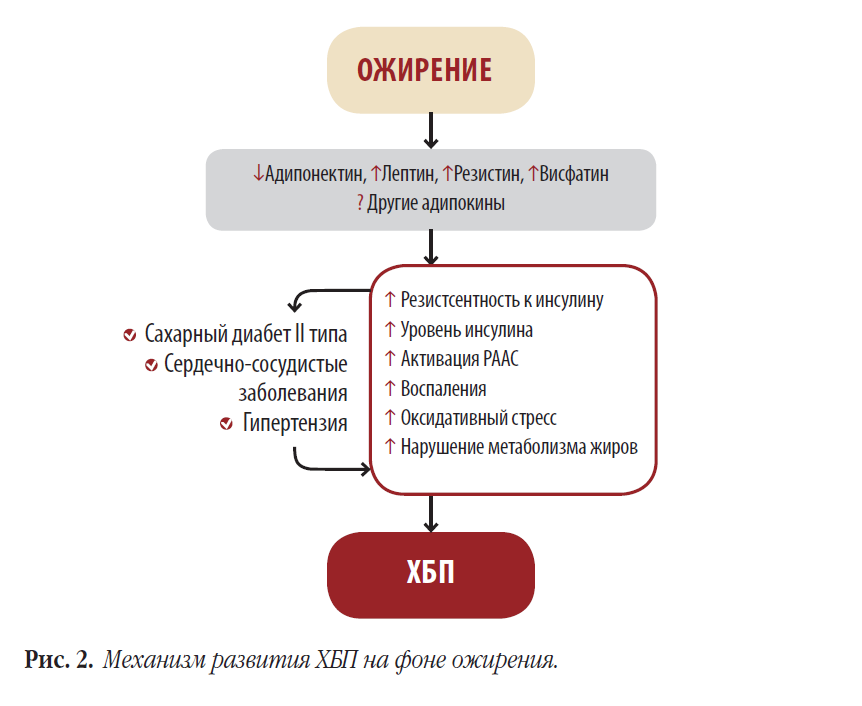
Избыточная активация ренин-ангиотензин-альдостероновой системы (РААС) способствует развитию гломерулопатии, ассоциированной с ожирением. Таким образом, в основе общего патогенеза ожирения и ХБП лежит ряд гуморальных нарушений, которые проявляются в усилении воспалительных реакций, избыточной активации ренин-ангиотензин-альдестероновой системы (РААС), формировании резистентности к инсулину и нарушении кишечной флоры.
Профилактика и лечение ожирения
Но все же есть и хорошие новости, отмечают Csaba P. Kovesdy et al. в статье, посвященной данной проблематике. «Главное, что само ожирение хорошо поддается профилактике», — говорить эксперт. По словам N.O. Savaria Camara, диета остается основным способом модификации кишечной микробиоты: потребление клетчатки способствует росту бактерий, продуцирующих короткие цепи жирных кислот. Однако подход к изменению образа питания должен быть грамотным, профессиональным. Так, согласно рекомендациям Национального института здоровья США (NIH), диета должна быть дефицитарной на 500–1000 ккал в день; необходима физическая нагрузка — 45 мин умеренной физической активности 5 дней в неделю.
Однако наибольшая трудность заключается в поддержании достигнутого веса в последующем. Неутешителен тот факт, что до 90% пациентов возвращаются к первоначальному весу в течение 2 лет. В связи с этим необходимо, наряду с поведенческими стратегиями, разрабатывать иные подходы к лечению и профилактике ХБП на фоне ожирения.
Большинство экспертов солидарны в том, что бариатрическая хирургия может стать весьма эффективным методом лечения пациентов с гломерулопатией, обусловленной ожирением. Основными предпосылками к этому служат:
непосредственная взаимосвязь между метаболическими нарушениями при ожирении и ХБП;
снижение веса, контроль глюкозы, улучшение качества жизни;
модификация кишечной микробиоты.
Несмотря на обилие работ, посвященных эффективности бариатрической хирургии в отношении ХБП, в настоящее время наблюдается отсутствие крупных рандомизированных исследований с достаточным периодом наблюдения, которые позволили бы официально рекомендовать этот метод лечения как основной [5].
Медикаментозное лечение
Медикаментозное лечение, и актуальное, и потенциально возможное, включает в себя применение таких препаратов, как ингибиторы ангиотензинпревращающего фермента (АПФ), антагонисты альдостероновых рецепторов, метформин, эмпаглифлозин, а также ряд фармакологических агентов, в настоящее время проходящих исследования.
Ингибиторы АПФ и антагонисты альдостероновых рецепторов давно зарекомендовали себя при лечении диабетической нефропатии. По мнению Zhi-Hing Liu, директора Национального научно-исследовательского центра заболеваний почек в Китае, препараты данной группы в комплексе со снижением веса должны быть главными методами лечения ХБП, индуцированной ожирением.
Более спорным считается вопрос об использовании противодиабетических препаратов метформина и эмпаглифлозина. Группой исследователей во главе с Malin S.K. продемонстрировано положительное влияние метформина на метаболизм пациентов с ожирением. Согласно данным Christensen M. и других авторов, применение метформина способствовало уменьшению воспаления, степени повреждения собирательных трубочек и препятствовало фиброзу почечной ткани. Использование метформина может быть потенциально полезно при гломерулопатии ожирения, однако следует учитывать риски развития лактат-ацидоза и проводить мониторинг состояния пациента.
Достаточными данными в отношении эмпаглифлозина, ингибитора натрийзависимого переносчика глюкозы 2-го типа, ученые пока не располагают. Данный гипогликемический препарат эффективен в отношении снижения прогрессирования ХБП у пациентов с сахарным диабетом 2-го типа и высоким кардиоваскулярным риском. Тем не менее механизм влияния эмпаглифлозина на почки в настоящее время до конца не изучен.
К потенциально перспективным решениям терапии ХБП на фоне ожирения ученые относят активатор фактора, индуцированного гипоксией, ингибиторы пролин-гидроксилазы, ингибитор апоптоза макрофагов, адипокины, а также биохимические факторы воздействия на митохондрии.
Другим вариантом терапии может быть фекальная трансплантация, зарекомендовавшая себя при угрожающем жизни колите, вызванном Clostridium Difficile. Идея данного метода лечения основана на концепции взаимосвязи патофизиологических механизмов нарушения кишечной флоры и развития гломерулопатии при ожирении.
В работе голландской группы исследователей, опубликованной в 2012 г. в издании Gastroenterology, продемонстрировано, что пересадка кишечной микрофлоры от худых реципиентов донорам с ожирением вызывала у последних снижение резистентности к инсулину [6]. Очевидно, что в отношении данного интересного метода также требуется проведение дополнительных рандомизированных исследований.
Заключение и вопросы
Дальнейшие успехи в понимании взаимосвязи между ожирением и ХБП зависят от возможности ответить на ряд вопросов, касающихся патофизиологии 2 состояний.
По мнению N.O. Savaria Camara, необходимо установить, какие именно факторы влияют на возникновение ХБП при ожирении. Известно, что не у всех пациентов с ожирением развивается почечная недостаточность. Методом лонгитюдного исследования установлено, что графическое отображение зависимости между ИМТ и развитием терминальной почечной недостаточности имеет форму параболы. То есть развитие терминального состояния не имеет линейной зависимости от ИМТ, и дефицит массы тела — также плохой прогностический фактор. Эксперты отмечают необходимость лучше понимать трехстороннюю взаимосвязь между кишечной микробиотой, ожирением и ХБП. Более того, необходимо подтвердить эффективность таких видов лечения, как бариатрическая хирургия, физическая активность, применение пробиотиков и диет, направленных на увеличение роста бактерий, продуцирующих короткие цепи жирных кислот.
По общему мнению экспертов, наблюдается ощутимый дефицит рандомизированных контролируемых исследований в данной области нефрологии. Перспективно в рамках современных тенденций направление, связанное с изучением генетических основ развития ХБП. Определение генетической предрасположенности может стать основой для индивидуального консультирования пациентов в зоне риска и разработки стратегии профилактических мер.
Пока же основной рекомендацией остается соблюдение базовых правил здорового образа жизни.
«Урология сегодня» 1(46)
1. Hsu C. Y., McCulloch C. E., Iribarren C., Darbinian J. & Go A. S. Body mass index and risk for end-stage renal disease. Ann. Intern. Med. 144, 21–28 (2006).
2. Fouque D. et al. A proposed nomenclature and diagnostic criteria for protein-energy wasting in acute and chronic kidney disease. Kidney Int. 73, 391–398 (2008).
3. https://www.kidney-international.org/article/S0085-2538(16)30620-2/pdf
4. Hunley T. E., Ma L. J. & Kon V. Scope and mechanisms of obesity- renal disease. Curr. Opin. Nephrol. Hypertens. 19, 227–234 (2010).
5. Run Li, Jianan Zou et al. Effects of bariatric surgery on renal in obese patients: a systematic review and analysis. PLoS ONE. 2016; 11 (10): e0163907.
6. Vrieze A. et al. Transfer of intestinal microbiota from lean donors increases insulin sensitivity in individuals with bolic syndrome. Gastroenterology 143, 913–916.e7 (2012).
Оценить
Средняя: 5,00 (1 оценка)
Источник
Мочекаменная болезнь и ожирение: есть ли взаимосвязь?
Несмотря на достигнутые успехи медицины, заболеваемость мочекаменной болезнью возрастает. В это же время человечество настигает «эпидемия XX1 века» — ожирение. Логично, что многие исследователи пытаются обосновать причинно-следственную связь между двумя этими нозологиями.
Ожирение как изменяемый фактор риска МС
Европейские урологи в последних исследованиях предположили, что ожирение может быть связано с повышенным риском развития мочекаменной болезни. Установлено, что, если индекс массы тела (ИМТ) выше 30 кг/ м², риск нефролитиаза значительно увеличивается. Важно отметить, что ожирение может быть связано с хронической почечной недостаточностью, сахарным диабетом, гипертонией и нефротическим синдромом.
Ожирение рассматривается как изменяемый фактор риска для заболеваний почек, оно связано с увеличением скорости клубочковой фильтрации и эффективного потока плазмы, опосредованных приростом фильтрационной фракции и экскрецией альбумина. Различные исследования показали, что это первые изменения в почечной функции, связанные с ожирением. Интересно, что ожирение также связано с увеличением удельного веса органа. Кроме того, с заболеванием связана гломерулопатия и фокальный сегментный гломерулосклероз.
Особенности обмена веществ при метаболическом синдроме (МС-резистентность к инсулину, дисгликемия, дислипидемия, гипертония и центральное ожирение) являются факторами риска не только для сердечно-сосудистых заболеваний, но и заболеваний почек. Нефролитиаз в анамнезе примерно в два раза чаще встречается у лиц с тремя критериями МС и в три раза чаще с пятью признаками. Взаимосвязь ожирения и других компонентов метаболического синдрома состоит в образовании камней через различные патофизиологические механизмы, включая увеличение экскреции оксалатов в моче, увеличение производства мочевой кислоты и дефектов аммониогенеза.
Ожирение также связано с уменьшением рН мочи: пациенты с более высоким ИМТ, как было обнаружено, имеют более низкий рН мочи и более высокую частоту возникновения уратов, оксалатных и фосфатных камней. Механизмы включают увеличение титруемой кислоты и уменьшение оснований в виде аммония и цитрата, что приводит к более высокой концентрации ионов водорода и закислению мочи.
Слабый пол и ожирение
Одна из наиболее ярких новых тенденций — увеличение числа случаев образования камней у женщин. Хотя нефролитиаз по-прежнему чаще встречается у мужчин, соотношение показателя заболеваемости мужчин к женщинам с камнями мочевыводящих путей сократилось с 3,4 до 1,3. Одна из гипотез для непропорционального увеличения мочекаменной болезни (МКБ) у женщин связана с ожирением, страдающие от избыточной массы тела женщины более склонны к развитию камней, чем мужчины с ожирением.
Ожирение и вид камней
Процент уратных и оксалатных камней при ожирении выше, чем у пациентов с нормальной массой тела. При исследовании было обнаружено преобладание оксалатных камней кальция у пациентов с ожирением — 34,9%, по сравнению с долей в 23,1% у пациентов с нормальным весом. Аналогичным образом распространенность камней мочевой кислоты составляет 7,7% для группы с ожирением и 2,8% для группы нормального веса. Интересно, что при исследовании 27 980 случаев МКБ с ожирением с 1976 по 2001 год и анализа состава конкрементов с помощью инфракрасной спектроскопии обнаружено, что женщины, как правило, имеют большую долю фосфатных и струвитных камней, предположительно из-за увеличения восприимчивости к инфекции мочевых путей. То же исследование показало, что распространенность камней мочевой кислоты имеет тенденцию к увеличению с возрастом для обоих полов. Связь между ожирением и увеличением экскреции оксалата была отмечена только у женщин и, наоборот, увеличение экскреции кальция было связано с ожирением у мужчин, но не было отмечено у женщин.
Белковое питание и нефролитиаз
Повышенное потребление животного белка может также способствовать подкислению мочи посредством повышения приема и выделения серосодержащих аминокислот, уменьшающих рН мочи. Увеличение приема пищи, богатой белком способствует развитию гиперурикозурии. Мочевая кислота более растворима в нейтральных или основных растворах, чем в кислых. Следовательно, так как рН мочи понижается, растворимость мочевой кислоты при уменьшении объемов мочи способствует большей вероятности кристаллизации, особенно в пересыщенных растворах. Оксалат, соединение, наиболее часто обнаруживаемое в кальцийсодержащих камнях, — еще одно литогенное соединение, что делает гипероксалурию фактором риска, общим для нефролитиаза для пациентов с ожирением, МС и сахарным диабетом 2 типа (СД), предрасположенным к гипероксалурии и низким рН мочи. Эти факторы, в особенности усугубленные обезвоживанием, могут стимулировать нефролитиаз.
Ожирение, гипертензия и камнеобразование
Гипертензия, а также другие метаболические изменения, связанные с ожирением, могут привести к образованию камней. В эпидемиологических исследованиях гипертония связана с повышенной частотой МКБ, независимо от возраста, массы тела или функции почек. В исследовании, проведенном в Университете Неаполя, в частности, было установлено, что распространенность мочекаменной болезни у исследуемых гипертоников составила 32,8% по сравнению с 13,4% у нормотензивной группы контроля. В более позднем перспективном исследовании в течение 8 лет наблюдения у 16,7% мужчин образовались конкременты по сравнению с 8,5% мужчин с нормальным давлением. Явная диспропорция говорит о том, что гипертония — прогностический фактор для возникновения мочекаменной болезни, а не возникает как следствие повреждения почек после образования конкрементов.
Ожирение, инсулинорезистентность и нефролитиаз
Важно отметить, что ожирение, как правило, ассоциируется с инсулинорезистентностью, которая изменяет почечный кислотно-щелочной обмен веществ, что приводит к снижению рН мочи (вызванное снижением производства аммиака) и повышенному риску осаждения мочевой кислоты, несмотря на нормоурикозурию. Большое количество исследований показали связь между МКБ и сахарным диабетом 2 типа с риском почечной недостаточности. Диабет и мочекаменная болезнь имеют двунаправленную связь: СД увеличивает риск развития МКБ и увеличивается в распространенности у пациентов с мочекаменной болезнью. В наблюдении камневыделители с диабетом 2 типа демонстрируют значительно большую долю оксалатов в моче при значительно более низком рН мочи, чем люди без диабета.
В ретроспективном исследовании однофакторный анализ показал, что больные СД ежедневно выводят меньше калия, фосфата и креатинина при значительно сниженном рН суточной мочи, а также наблюдается пониженная кальций-фосфатная пресыщенность. Регрессионный анализ выявил, что СД 2 типа — самый выраженный независимый фактор риска образования камней мочевой кислоты. Кроме того, неконтролируемый СД был связан с более высокой распространенностью МКБ. Таким образом, пациенты с камнями мочевой кислоты и избыточным весом должны быть обследованы для выявления диабета и компонентов метаболического синдрома.
В крупном общенациональном обзоре нефролитиаза в Японии выявили, что дислипидемия связана с увеличением частоты рецидивирующих или множественных камней независимо от возраста, пола или при наличии других признаков МетС. Концентрации липидных компонентов сыворотки коррелируют с изменениями в моче. Высокий уровень общего холестерина предполагает значительно более высокий уровень калия и кальция в моче, в то время как низкий уровень ЛПВП или высокий уровень триглицеридов коррелировал с повышенным количеством натрия, оксалатов и мочевой кислоты.
МКБ у детей с ожирением
Другая тревожная тенденция — увеличение числа случаев почечнокаменной болезни в педиатрической популяции. При оценке 25-летнего периода выявлен прирост мочекаменной болезни на 4% в год в значительной степени из-за роста заболеваемости в 12-17-летней возрастной группе. Интересно, что, согласно анализу, доля мальчиков, страдающих МКБ, выше в первые 10 лет жизни, а далее наблюдают преобладание заболевших девочек.
В большинстве случаев мочекаменная болезнь у детей имеет идиопатическую этиологию, по разным данным, лишь у 9-24% возможно идентифицировать причину: нарушение метаболизма, нейрогенные факторы или врожденные аномалии мочевыделительной системы. Есть некоторые особенности МКБ и метаболических параметров у детей. Хотя образование конкрементов имеет линейную связь с возрастом пациента, педиатрические пациенты, как правило, образуют больший процент камней на основе кальция и меньший — уратов, чем взрослые. Причина такого несоответствия связана с более высоким рН мочи в педиатрической популяции, чем у взрослых.
С ростом детского ожирения высокий ИМТ уже давно предполагается как весомый фактор в педиатрической эпидемии мочекаменной болезни. Однако исследователи дают противоречивую оценку. Пациенты с более низким процентилем веса тела имеют более раннюю манифестацию болезни. Самый высокий процент маленьких пациентов с МКБ принадлежит к нормальной весовой категории (49,1% против 41,1% с избыточной массой). Кроме того, ожирение не увеличивает риск развития конкрементов большего размера или потребность в дополнительных хирургических манипуляциях по сравнению с другими весовыми категориями. В исследовании случай—контроль сообщили об отсутствии связи между высоким ИМТ и мочекаменной болезнью у детей. Отсутствие убедительных доказательств, связывающих ожирение и МКБ, приводит к гипотезе, что, возможно, изменения в диете, а не ИМТ выступают в качестве виновника мочекаменной болезни у детей. Сообщается, что уровень мочевой кислоты и оксалатов коррелирует с долей жира в организме и свободными глюкокортикоидами. Кальций в моче связан с пищей, богатой натрием и белком, но не ИМТ у здоровых детей.
Согласно отчету Института медицины США 2010 года, среднее диетическое потребление натрия детьми в возрасте 6-11 лет увеличилось с 200 мг в 1970-х до 3000 мг в 2000-е годы. Гипертония, как было обнаружено, является существенным фактором риска развития почечнокаменной болезни у детей в возрасте 10 лет и младше, в то время как сахарный диабет выступает фактором риска для детей в возрасте до 5 лет. В попытке определить факторы риска в моче у педиатрических пациентов с МКБ выявлена гиперкальциурия как принципиальное отличие между формированием конкрементов у детей. Удивительно, но другие мочевые характеристики, связанные со взрослыми факторами образования камня, а именно низкий объем мочи, гипероксалурия, гипоцитратурия и низкий рН мочи не представлены в качестве основных факторов риска в формировании камней у детей.
Выход есть
Медикаментозное лечение ожирения и изменение образа жизни — два ключевых момента в лечении этого заболевания. Борьба с абдоминальным ожирением и резистентностью к инсулину и снижение частоты сердечно-сосудистых осложнений и развитие сахарного диабета могут улучшить эффективность терапии МКБ, осложненной ожирением. В литературе достоверно продемонстрировано, что ожирение связано с высокой частотой осложнений до, во время и после хирургических вмешательств. Бариатрическая операция к тому же весьма дорогая, рассматривается в качестве последнего эффективного метода в поддержании значительной потери веса при ожирении.
Источник